ФОРМАЛЬДЕГИД (муравьиный альдегид, метаналь), HCHO, мол. м. 30,3; бесцветный газ с резким раздражающим запахом; т. пл. -118 0C, т. кип. -19,2 0C; d-804 0,9172,d-204 0,8153, плотн. по воздуху 1,04; tкрит 137,2-141,2 0C, ркрит 6,784-6,637 МПа; ур-ние температурной зависимости давления пара в интервале от -109 до -220C: lg r (Па) = 9,2817 - 959,437(243,39 + t); Сор 35,4 Дж/(моль · К),∆Нисп 23,31 кДж/моль (19 0C), ∆H0сгор-561,5 кДж/моль,∆ Н0обр-115,9 кДж/моль,S0298218,8 Дж/(моль · К).
Чистый газообразный Ф. относительно стабилен при 80-100 0C, при т-рах ниже 80 0C медленно полимеризуется; процесс ускоряется в присутствии полярных растворителей (в т.ч. воды), кислот и щелочей.
Ф. хорошо раств. в воде, спиртах и др. полярных р-рителях. При низких т-рах смешивается в любых соотношениях с неполярными р-рителями: толуолом, диэтиловым эфиром, этилацетатом, CHCl3 (с увеличением т-ры р-римость падает), не раств. в петролейном эфире. Водные р-ры Ф. содержат равновесную смесь моногидрата CH2(OH)2 (99,9%), неустойчивого в своб. состоянии, и полимергидратов HO(CH2O)nH (п = 2-8), устойчивых кристаллич. соединений. При продолжит. хранении водных р-ров (особенно при низких т-рах) и при их концентрировании степень полимеризации увеличивается. Для хранения водных р-ров Ф. их стабилизируют метанолом (см. Формалин). При упаривании водных р-ров в вакууме образуется параформ, или параформальде-гид (CH2O)n (п = 8-12), при действии щелочи на конц. водные р-ры - т. наз. a-полиоксиметилен (n > 100). Полимеризация в неполярном р-рителе приводит к полиформальдегиду (n > 1000).
Параформ - бесцв. кристаллы с запахом Ф., т. пл. 120-170 0C, в холодной воде р-ряется медленно, в горячей -быстро, образуя р-ры Ф., плохо раств. в ацетоне; горюч, т. всп. 720C. 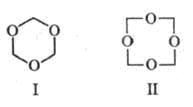
Известны циклич. полимеры Ф.: триоксан (ф-ла I, т. пл. 64 0C), получаемый перегонкой 60%-ного водного р-ра Ф. с разб. H2SO4, и тетраоксиметилен (ф-ла II, т. пл. 112 0C), образующийся при нагр. диацетата высокомол. полиоксиметилена.
Ф. обладает высокой реакционной способностью. Восстанавливается H2 в присут. многих металлов или их оксидов (напр., Ni, Pt, Cu) до метанола; окисляется HNO3, KMnO4 до муравьиной к-ты или CO2 и H2O; осаждает мн. металлы (Ag, Pt, Au, Bi и др.) из р-ров их солей, окисляясь при этом в муравьиную к-ту.
С альдегидами в присут. сильных щелочей Ф. вступает в т. наз. перекрестную р-цию Канниццаро (C6H5CHO + HCHO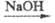 C6H5CH2OH + HCOONa); с ацетальдегидом в присут. Ca(OH)2 образует пентаэритрит, в паровой фазе при 285 0C - акролеин; под действием алкоголятов Al или Mg Ф. подвергается диспропорционированию с образованием ме-тилфомиата (см. Тищенко реакция). C6H5CH2OH + HCOONa); с ацетальдегидом в присут. Ca(OH)2 образует пентаэритрит, в паровой фазе при 285 0C - акролеин; под действием алкоголятов Al или Mg Ф. подвергается диспропорционированию с образованием ме-тилфомиата (см. Тищенко реакция).
Р-ция Ф. со спиртами в присут. сильных к-т приводит к ацеталям (формалям), с H2S - к циклич. тритиану, с HCN в присут. щелочей - к циангидрину:
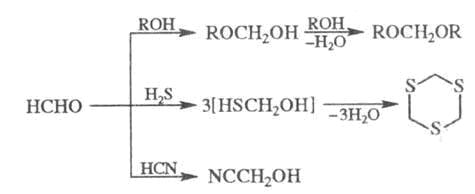
Ф. присоединяется к олефинам в присут. кислых катализаторов с образованием 1,3-дигликолей и 1,3-диоксанов (см. Принса реакция), р-ция Ф. с изобутиленом дает изопрен, жидкофазная конденсация с пропиленом в присут. BF3 или H2SO4 - бутадиен. Из Ф. и кетена в пром-сти получают b-пропиолактон.
Р-ция Ф. с ацетиленом - пром. способ получения бутадиена (см. Рeппe реакции), при взаимод. двух молекул Ф. с ацетиленом образуется 2-бутин-1,4-диол.
В присут. извести Ф. превращается в углеводы:
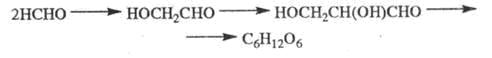
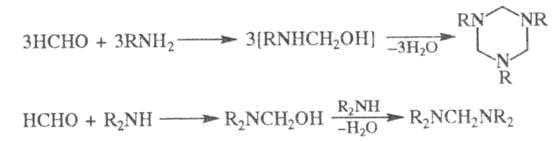
При взаимод. Ф. с NH3 образуется гексаметилентетрамин, с первичными аминами - тримеры, с вторичными - бис-(ди-алкиламино)метаны:
Соед. с подвижным атомом водорода реагируют с Ф. и NH3 (или аминами) по Манниха реакции. Р-ция Ф. с NH4Cl пром. способ получения метиламина: 2НСНО + NH4Cl →CH3NH2 · HCl + HCOOH (р-ция может идти дальше с образованием ди- и триметиламинов). С мочевиной в щелочной среде Ф. дает моно- и диметилольные производные, поликонденсацией к-рых получают мочевино-формальдегидные смолы, а из меламина и Ф.- меламино-формальдегидные смолы.
Ароматич. соед. (бензол, анилин, толуол) образуют с Ф. соответствующие диарилметаны; в присут. HCl бензол хлор-метилируется Ф. по Блана реакции, образуя бензилхлорид; с фенолами в присут. к-т или оснований Ф. конденсируется с образованием орто- и пара-метилольных производных, к-рые далее превращаются в феноло-формалъдегидные смолы. Продукты конденсации Ф. с фенол- и нафталинсульфокислотами используют как дубильные в-ва (неразол и др.).
В промышленности Ф. получают окислит. дегидрированием метанола в паровой фазе O2 воздуха в присут. Ag при 680-720 0C (конверсия метанола 97-98%) либо в присут. Ag или серебряной сетки при 600-650 0C (конверсия 77-87%) с возвращением непрореагировавшего метанола в рецикл. Процесс можно проводить в избытке воздуха в присут. оксидов металлов (Fe-Mo-V) при 250-400 0C (конверсия 98-99%). Ф. может быть получен окислением метана, пропана, бутана, этилена, гидрированием СО, однако эти методы не имеют промышленного значения по экономическим причинам.
В лаб. условиях Ф. получают дегидрированием метанола над медью, термич. разложением формиата цинка, деполимеризацией параформа.
Дня обнаружения Ф. используют реагент Шиффа или р-цию Ф. с фенилгидразином и K3[Fe(CN)6] в щелочной среде (красное окрашивание). Определяют Ф. иодометрически либо применяют р-цию Ф. с сульфитом Na с послед. титрованием выделившейся щелочи к-той: HCHO+ Na2SO3→HOCH2SO3Na + NaOH, а также жидкостной хроматографией и др. методами.
Ф. используют в орг. синтезе, в произ-ве синтетич. смол и пластмасс, для синтеза мн. лек. в-в и красителей, для дубления кож, как дезинфицирующее, антисептическое и дезодорирующее средство.
Ф. токсичен, вызывает дегенеративные процессы в паренхиматозных органах. Сильное действие на нервную систему, по-видимому, связано с наличием примесей метанола в техн. Ф. или превращением Ф. в организме в метанол и муравьиную к-ту. В то же время считается, что Ф. быстро окисляется в организме до CO2 (на 70-80%).
ПДК в атм. воздухе 0,003 мг/м3, в воздухе рабочей зоны 0,5 мг/м3, в воде водоемов хозяйственно-бытового пользования 0,05 мг/л. T. самовоспл. 430 0C, КПВ при 20 0C 7-72% (по объему).
Мировое производство Ф. ок. 5 млн. т в год (1980), из них в США 28%, Германии 17%, Японии 12%.
| 









